Hinweis: Dieser Artikel ist ein Beitrag zum ScienceBlogs Blog-Schreibwettbewerb 2015. Hinweise zum Ablauf des Bewerbs und wie ihr dabei Abstimmen könnt findet ihr hier. Informationen über die Autoren der Wettbewerbsbeiträge findet ihr jeweils am Ende der Artikel.

——————————————
Der Leipziger Fockeberg ist eine Trümmerkippe, auf der es an milden Sommernächten überall grün leuchtet. Die spektakuläre Erscheinung hat eine ganz natürliche Ursache: Der 150 Meter hohe Schuttberg ist mittlerweile an die 70 Jahre alt, bewaldet, und es wimmelt dort von Glühwürmchen. Besonders Ende Juni finden sich dort Hunderte der kleinen Leuchtkäfer und tragen sicherlich zur romantischen Stimmung bei, die fast ebenso viele Menschen aus den umliegenden Stadtteilen Abend für Abend dort hinauf lockt.
Warum aber leuchten die Käfer eigentlich? Was bezwecken sie damit, und wie kriegen sie das hin? Und warum leuchten die nicht auch mal weiß oder lila oder blau?

Glühwürmchen im Wald (Bild: Quit007, CC-BY-SA 3.0)
Biolumineszenz
Dass Lebewesen Licht erzeugen können, ist ein verbreitetes Phänomen namens Biolumineszenz (bios = Leben, lumen = Licht). Wir bekommen nur so selten etwas davon mit, weil die meisten leuchtenden Organismen im Wasser leben. In Meerestiefen ab 700 m gehört es sogar zum guten Ton: Bis zu 90 % der bekannten Lebensformen dort produzieren ihr eigenes Licht. Es sind leuchtende Fische bekannt, Quallen, Krebse und vor allem Einzeller. Diese sind auch häufig als nützliche Untermieter in den Leuchtorganen höherer Lebewesen zu finden. An Land sind es hauptsächlich einige Insekten- und Pilzarten, die leuchten können.
Der biologische Zweck des Leuchtens ist vielfältig: Manche (wie die Glühwürmchen) machen mögliche Partner auf sich aufmerksam, Tiefsee-Anglerfischen geht es eher um Beute. Der Vampirtintenfisch führt potentielle Räuber in die Irre, indem er eine Wand aus leuchtenden Partikeln ausstößt und sich dann aus dem Staub macht. Auf einer Privatfrequenz kommunizieren die Tiefseefische der Gattung Malacosteus: Das von ihnen ausgesendete rote Licht befindet sich in einem Wellenlängenbereich, den die meisten anderen Tiefseeorganismen gar nicht wahrnehmen können.
Bei vielen Lebewesen ist aber noch nicht abschließend geklärt, was die Leuchterei bezwecken soll. Im Zweifelsfall sollen Freunde angelockt oder Feinde in die Irre geführt werden.
Und wie funktioniert diese Biolumineszenz jetzt?
Zunächst einmal handelt es sich um ein nicht-thermisches Leuchten, das durch eine chemische Reaktion hervorgerufen wird. Das Glühwürmchen bleibt dabei also kalt und hat streng genommen seinen Namen verfehlt. Damit der Käfer leuchten kann, braucht es eine
chemische Umwandlung mit folgenden Eigenschaften: Es müssen anregbare Elektronen im Spiel sein (keine Sorge, das wird gleich erklärt), die dabei erzeugte Strahlungsenergie muss sich im Bereich des sichtbaren Lichts befinden, und es sollten möglichst wenige unerwünschte Nebenprodukte anfallen, die uns die Lichtausbeute vermiesen.
Und was sind bitte anregbare Elektronen?
Damit hat es folgendes auf sich: Jedes Atom hat eine Hülle aus Elektronen (negativ geladene Teilchen), die um den positiv geladenen Kern herumschwirren. Wie viele Elektronen das sind, hängt davon ab, um welche Atomsorte es sich handelt. Im Fall von Sauerstoff sind das zum Beispiel 8. Diese 8 Elektronen sind nicht einfach irgendwie unsortiert unterwegs, sondern jedes hat sein bestimmtes sogenanntes Energieniveau. Eventuell mitlesende Quantenmechaniker werden gleich ohnmächtig vom Stuhl kippen, aber stellen wir uns das vereinfacht mal so vor, als wäre jedes Elektron eine Art Satellit, das den kugelförmigen Atomkern wie einen Planeten umkreist. Das erste und zweite Elektron sind ganz nah dran, das dritte bis achte weiter draußen. Je weiter ein Elektron vom Kern entfernt ist, umso schneller saust es um ihn herum: Es hat ein höheres Energieniveau. Wenn jetzt eins dieser äußeren Elektronen noch einen zusätzlichen Schubs kriegt, kann es für kurze Zeit auf einem noch höheren Energieniveau fliegen, es hat seinen Grundzustand verlassen und ist angeregt. Dieser Schubs kann in Form von Bestrahlung, also Lichtenergie, zugeführt werden, oder thermisch, oder aber Folge einer chemischen Umwandlung sein.
Niemand ist allerdings gerne auf Dauer angeregt, deshalb kehren die meisten Systeme nach kurzer Zeit wieder zu ihrem Grundzustand zurück. Solche Übergänge zwischen Energiezuständen bzw. -niveaus hat man früher auch als Quantensprünge bezeichnet. Was also häufig als Umschreibung für einen ganz großen Wurf herhalten muss, ist in Wirklichkeit keine große Sache, jedenfalls nicht aus Sicht eines Leuchtkäfers.
Moleküle sind nichts anderes als Zusammenschlüsse von mehreren Atomen zu einem neuen Stoff. Und die Strukturformel des Stoffes, mit dem unsere Glühwürmchen arbeiten, ist in der folgenden Abbildung zu sehen. Es handelt sich um ein sogenanntes Luciferin („Lucifer“ ist der Lichtträger), das für angeregte Zustände durchaus zu haben ist, wie wir gleich noch sehen werden.
Das sieht jetzt erst einmal relativ wild aus, soll uns aber nicht weiter abschrecken. Wir sehen hier eine Struktur aus 11 Kohlenstoffatomen (C), 3 Sauerstoffatomen (O), je 2 Atomen Stickstoff (N) und Schwefel (S) sowie 8 Wasserstoffatomen (H).
Wichtig ist im ersten Schritt nur die Gruppe rechts unten, die wir rot markiert haben, denn da geht es gleich zur Sache: Dort hängt eine sogenannte Carboxylgruppe, die aus einem Kohlenstoffatom, zweimal Sauerstoff und einmal Wasserstoff besteht. Die Striche zwischen den Atomen sind Bindungen; doppelte Striche sind Doppelbindungen, zwischen zwei Kohlenstoffatomen werden sie auch gerne als ungesättigt bezeichnet – den Ernährungsbewussten unter uns keine Unbekannten.
Die Carboxylgruppe ist über eine einfache Bindung mit dem benachbarten Ring verbunden. Die linke Seite des Moleküls nimmt die gleich folgenden Vorgänge eher unbeteiligt zur Kenntnis, weshalb wir sie der Übersichtlichkeit halber nicht weiter mitbetrachten.
Ihr kennt die Carboxylgruppe besser, als ihr denkt: wann immer wir so einer Gruppe in einem organischen Molekül begegnen, haben wir es mit einer Säure zu tun! Essigsäure, Apfelsäure, Fettsäuren, Aminosäuren, Buttersäure, Zitronensäure… die Liste ist beliebig lang, und sie alle haben mindestens eine solche Gruppe aus einem Kohlenstoff, zwei Sauerstoffen und einem Wasserstoffatom aufzuweisen.
Von der Säure zur Erleuchtung
Das Glühwürmchen macht nun folgendes: Als erstes produziert es ein Enzym namens Luciferase. Enzyme sind natürliche Katalysatoren, die in allen Lebewesen eine wichtige Rolle spielen, denn sie zwingen die Moleküle in unseren Zellen dazu, die jeweils erwünschte chemische Reaktion durchzuführen – sie kontrollieren unseren gesamten Stoffwechsel. Dabei handelt es sich oft um Umwandlungen, die ohne Katalysator überhaupt nicht funktionieren würden, erst recht nicht bei den milden Temperaturen und pH-Werten, die in einem Organismus so vorherrschen.
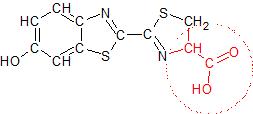
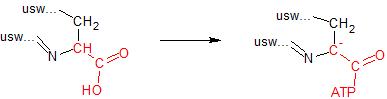
Unsere Luciferase also ist ein riesiger Naturstoff, der aus Tausenden von Atomen besteht und so ein kleines Molekül wie das Luciferin komplett umhüllen kann. Es hält das Luciferin an mehreren Stellen gut fest und reißt ihm den größten Teil seiner Säuregruppe ab, nämlich ein Sauerstoffatom und ein Wasserstoffatom sowie bei der Gelegenheit auch noch einen zusätzlichen Wasserstoffkern aus dem benachbarten Ring. Das sieht dann in etwa so aus:
Ich habe gerade Wasserstoffkern gesagt, und das war kein Versehen: Das Wasserstoffatom hat sein Elektron zurückgelassen, deshalb ist unser Molekül plötzlich negativ geladen! Diesen Vorgang nennt man auch Deprotonieren (es wird ein Proton, also das, was vom Wasserstoff ohne Elektron noch übrig ist, entfernt), und das ist das tägliche Brot von sogenannten Basen; Natronlauge oder Ammoniak zum Beispiel deprotonieren den ganzen Tag andere Stoffe und sind deshalb auch so ein beliebtes Reinigungsmittel für harte Fälle.
„ATP“ steht, nebenbei bemerkt, für Adenosintriphosphat. Lasst euch davon nicht ablenken. Diese Substanz taucht ständig auf, wenn wir es mit Stoffwechselprozessen zu tun haben; an dieser Stelle sei nur kurz erwähnt, dass ATP eine Art universeller Energiespeicher ist.
Zurück zu unserem negativen Kohlenstoffatom: Das hat jetzt zu allem Übel auch nur noch drei Bindungspartner. Er hätte aber lieber vier – so ist der Kohlenstoff eben, und deshalb wird sofort das nächste verfügbare Sauerstoffmolekül gegriffen und dort angebaut (zum Glück gibt es immer Sauerstoff, denn der Leuchtkäfer hat inzwischen ganz ruhig weitergeatmet – der kennt das ja schon). Sauerstoffmoleküle werden nicht von ungefähr als Radikale bezeichnet, denn die haben ihren eigenen Kopf. Anstatt sich unauffällig einzufügen, bauen die O’s plötzlich ihren Privatring:
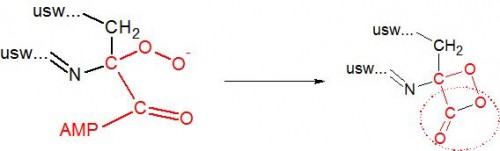
Das vorher negativ geladene Kohlenstoffatom bindet ein vorbeifliegendes Sauerstoffmolekül (O2), das im nächsten Schritt einen Ring bildet. Der eingekreisten Atomgruppe CO2 wird es gleich an den Kragen gehen.
Ringe aus vier Atomen sind sehr instabil, vor allem wenn darin zwei benachbarte Sauerstoffatome vorkommen. Die Bindungen zwischen den Atomen müssen hier plötzlich Winkel bilden, die ihnen eigentlich viel zu klein sind: Es herrscht eine gewaltige Spannung. Die Luciferase greift durch und stellt wieder Ordnung her, indem sie ein Kohlenstoffdioxidmolekül aus dem Ring schneidet und somit eine vereinfachte Version unseres Ursprungsmoleküls erhält, das Oxyluciferin:
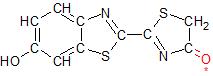
Die Luciferase hat das Luciferin zu Oxyluciferin umgewandelt. Der Stern markiert den angeregten Zustand, in dem das Molekül sich befindet
Und nun kommen wir endlich zum eigentlichen Zweck des ganzen Zaubers: Eines der Elektronen befindet sich noch auf einem Energieniveau, das für die instabilen Zwischenstufen ganz in Ordnung war, aber für unser Oxyluciferin viel zu hoch ist. Es saust sozusagen mit erhöhter Geschwindigkeit durch die Gegend und stellt plötzlich fest, dass inzwischen wieder Ruhe eingekehrt ist: Die Reaktion ist abgeschlossen und wir haben schon das Ortseinfahrtsschild passiert. Das Elektron beruhigt sich und kehrt zu seinem sogenannten Grundzustand zurück.
Dabei wird Energie frei, und diese Energie wird in Form von Licht abgegeben. Da der Unterschied zwischen dem angeregten und dem Grundzustand immer exakt gleich ist, hat das ausgestrahlte Licht auch immer exakt dieselbe Wellenlänge und wir sehen somit immer dieselbe Farbe. Zumindest bei ein und demselben Tier. Im Falle unseres Glühwürmchens liegt die übliche Wellenlänge im Bereich von 550 Nanometer, es leuchtet grün. Das entspricht in etwa einer Energiedifferenz von 2,25 Elektronenvolt, oder 218 Kilojoule pro Mol. Etwas veranschaulicht: Hätten wir 500 Gramm Glühwürmchenluciferin und würden diese komplett zum Leuchten bringen, würden wir bei einer Energie von etwa 390 Kilojoule landen. Mit dieser Energiemenge könnte man zum Beispiel 93 Milliliter Wasser um ein Grad erhitzen – nicht gerade beeindruckend. Vor allem, wenn man bedenkt, dass ein Glühwürmchen nur etwa 200 Milligramm wiegt. Es bräuchte also eine ganze Legion für ein halbes Kilogramm Leuchtstoff.
Für rotes Licht ist noch weniger Energie notwendig, während wir aber ein Stück Eisen auf über 800 °C erhitzen müssten, um eine hellrote Glühfarbe zu erreichen. Kein Wunder, dass die Tierwelt sich einvernehmlich für das kalte Leuchten entschieden hat.
Dass die Lichtfarben der Käfer usnd Quallen, Krebse und Fische, Pilze und Bakterien durchaus sehr unterschiedlich ausfallen, liegt immer an der speziellen Energiedifferenz zwischen angeregtem und Grundzustand. Aus mehreren Gründen variiert diese Differenz: Das Luciferin ist bei jeder Spezies unterschiedlich aufgebaut; die Luciferase des einen Käfers zerrt etwas stärker am Luciferin als die des anderen und sorgt damit für eine leicht unterschiedliche Elektronenenergie; auch der pH-Wert der Umgebung spielt eine Rolle. Manche Tiere machen es sich sogar noch komplizierter und schalten fluoreszierende Substanzen dazwischen, die das erzeugte Licht aufnehmen und in eine andere Farbe konvertieren. Das Grundprinzip ist aber überall dasselbe: Ein Luciferin wird von einer Luciferase erst deprotoniert, dann oxidiert und muss sich danach erstmal wieder abregen.
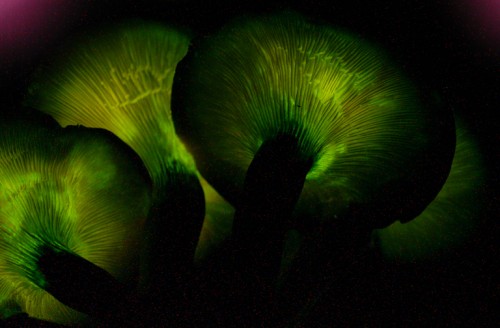
Leuchtende Ölbaumpilze (Bild: Noah Siegel, CC-BY-SA 3.0)
Die Effizienz dieses Vorgangs lässt dabei jeden LED-Hersteller vor Neid erblassen: Nahezu 100% Lichtausbeute kann der Leuchtkäfer vorweisen. Die Lichtintensität ist dabei freilich nicht so groß: In einem Meter Entfernung kommt pro Quadratzentimeter Rezeptorfläche nicht einmal mehr ein Nanowatt Lichtleistung an. Für die Abendstimmung also super, um den Nachhauseweg zu beleuchten eher nicht.
Jetzt will ich auch leuchten!
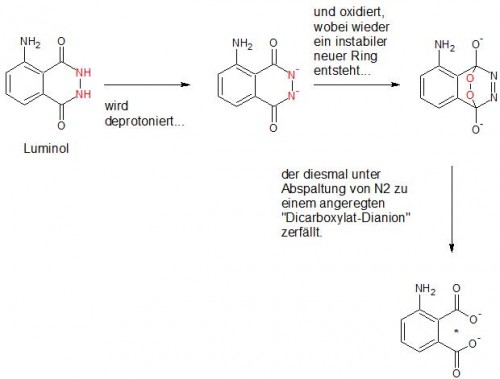
Wie wir gesehen haben, ist die Biolumineszenz Ergebnis einer chemischen Reaktion, die in lebenden Organismen stattfindet. Geht das denn auch ohne Käfer, Qualle oder Bakterium? Aber hallo! Ein beliebtes Experiment im Chemieunterricht, das man auch relativ gefahrlos zuhause ausprobieren kann, ist die sogenannte Luminol-Reaktion. Luminol ist ein gelbliches Pulver, das unter ganz ähnlichen Umständen wie das Luciferin zum Leuchten gebracht werden kann:
Auch hier brauchen wir also wieder als erstes eine Deprotonierung, als zweites eine Reaktion mit Sauerstoff (den uns hier ein Oxidationsmittel liefert), und schließlich einen instabilen Ring, der zu einem angeregten Molekül zerfällt, welches unter blauer Lichtabgabe in seinen Grundzustand zurückkehrt. Und ganz ähnlich wie beim Käfer funktioniert das alles nicht ohne Katalysator; auch wenn wir in diesem Fall kein kompliziertes Enzym brauchen, sondern lediglich ein Eisensalz (im Video an der gelben Farbe erkennbar):
Luminol hat übrigens sogar einen praktischen Nutzen: Da die Leuchtreaktion mit Hilfe von Eisenverbindungen in Gang gesetzt wird, lassen sich damit noch kleinste Blutspuren nachweisen. Wenn ihr es also das nächste Mal in einem Fernsehkrimi blaues Licht seht, wisst ihr jetzt ganz genau, was da passiert.
————————————————-
Hinweis zur Autorin: Dieser Artikel wurde von Nora verfasst, einer Chemikerin aus Leipzig.











Kommentare (21)