In letzter Zeit war ja öfter mal von negativen Temperaturen die Rede. Also nicht die negativen Temperaturen draußen, wo es aus irgendeinem Grund immer noch kalt ist und schneit, sondern negative absolute Temperaturen. Und merkwürdigerweise sollen die in Wahrheit gar nicht kalt sein, sondern heiß. Um zu verstehen, wie so etwas auf den ersten Blick absurdes gemeint sein kann, müssen wir uns erst einmal eine ganz grundlegende Frage stellen: Was ist überhaupt eine Temperatur?
Ich fange ganz fundamental an, nämlich mit den berühmten Hauptsätzen der Thermodynamik. Bekannt und viel zitiert ist der erste Hauptsatz der Thermodynamik, der sagt, dass die Energie in einem abgeschlossenen System konstant ist. Ebenfalls oft zitiert wird der zweite Hauptsatz der Thermodynamik, den es in verschiedenen Formulierungen gibt. Ich verwende heute die, die mit dem Entropiebegriff hantiert: “Die Entropie eines abgeschlossenen Systems erreicht im thermischen Gleichgewicht ihr Maximum.” (Für den Moment braucht ihr gar nicht genau zu wissen, was die Entropie ist, aber ich habe das na klar auch mal ausführlich erklärt (vielleicht sollte der Blog lieber “Hier wohnt der Erklärbär” heißen?) – klickt rechts auf Artikelserien und dort findet ihr eine mehrteilige Serie zum Thema (und inzwischen sollten die Links sogar wieder funktionieren…).)
Heute fange ich aber mit dem – wenig beachteten, weil für trivial gehaltenen – Nullten Hautpsatz an. den klaue ich wörtlich von Wikipedia:
Stehen zwei Systeme jeweils mit einem dritten im thermodynamischen Gleichgewicht, so stehen sie auch untereinander im Gleichgewicht. Diejenige Zustandsgröße, die bei diesen Systemen übereinstimmt, ist die Temperatur.
Der Satz sagt uns Folgendes: Systeme (unter einem System könnt ihr euch alles vorstellen, was eine Temperatur haben kann; Physikerinnen bevorzugen meist einfache Dinge wie Gase oder einigermaßen simpel aufgebaute Festkörper; gut ist auch immer ne Flasche mit Wasser oder eine Badewanne voll davon) – also: Systeme können im thermodynamischem Gleichgewicht sein. Das ist grob gesagt dann der Fall, wenn sie durch bestimmte Größen (beispielsweise den Druck in einem Gas oder sein Volumen) beschrieben werden können und wenn die sich zeitlich nicht mehr ändern. (Man kann das auch noch axiomatischer formulieren, aber die Physik ist ja keine axiomatische Wissenschaft, für mich reicht heute diese einfache Definition für den Hausgebrauch.)
Wenn ich zwei Systeme miteinander in Kontakt bringe, so dass sie Energie austauschen können, dann erreichen sie irgendwann ein thermodynamisches Gleichgewicht miteinander. Das erkenne ich daran, dass sie netto keine Energie mehr austauschen (obwohl statistisch durchaus mal ein bisschen Energie von einem zum anderen fließen kann, aber im Mittel gleicht sich das immer aus). Der Nullte Hauptsatz sagt mir nun, dass Wenn A mit B im Gleichgewicht ist und B mit C, dann ist auch A mit C im Gleichgewicht. Das bedeutet, dass es eine einzige Größe geben muss, mit der ich ein thermodynamisches Gleichgewicht kennzeichnen kann, und diese Größe ist gerade die Temperatur.
Klingt ein bisschen abstrakt, ist aber eigentlich ganz logisch. Bei der Körpergröße ist es zum Beispiel genauso: Wenn A genauso groß ist wie B und B so groß wie C, dann ist auch A so groß wie C. Es gibt deshalb eine Zahl, die die Körpergröße kennzeichnet. Bei anderen Dingen ist es aber nicht so: Wenn zum Beispiel A und B beim Schach immer remis spielen und B und C auch, dann heißt das nicht, dass A und C auch immer remis spielen müssen – die Spielstärke im Schach lässt sich nicht durch eine einzige Zahl kennzeichnen (auch wenn es natürlich ELO-Zahlen gibt).
Es gibt also eine Größe, die wir Temperatur nennen und die dazu dient, festzustellen, ob zwei Systeme im thermischen Gleichgewicht sind oder nicht. Wäre natürlich toll, man hätte eine Idee, was diese Größe eigentlich ist, oder? (Klar, aus dem Alltag könnte man – analog zu Einstein – sagen “Temperatur ist das, was ein Thermometer anzeigt”, aber hier schauen wir genauer hin…)
Dazu nehmen wir den ersten und zweiten Hauptsatz zur Hilfe. Wir betrachten zwei Systeme, die miteinander Energie austauschen können und die ansonsten von ihrer Umwelt isoliert sind. (Konkret könnt ihr wieder die Badewanne und die Wasserflasche nehmen, wenn ihr wollt.) Nach einer Weile werden die beiden Systeme (durch den Energieaustausch) im thermodynamischen Gleichgewicht sein (also dieselbe Temperatur haben). Die Energie des Gesamtsystems ändert sich laut erstem Hauptsatz nicht – es kann also nur Energie hin- und herfließen.
Wir fragen uns jetzt, wie die Energie sich auf die beiden Systeme verteilt. Hat das eine System viel Energie, das andere wenig? Oder bekommen beide gleich viel Energie ab? Man könnte ja versucht sein zu sagen, dass die Energie in beiden Systemen gleich sein muss (weil Temperatur ja etwas mit Energie zu tun hat), aber das stimmt natürlich nicht – wenn ich die Flasche mit Wasser in eine Badewanne halte, dann hat das Wasser in der Badewanne auch im thermodynamischen Gleichgewicht viel mehr Energie als das in der Flasche, weil einfach mehr Wasser da ist.
Statt lange herumzurätseln, wie sich denn nun die Energie verteilt, können wir aber einfach den 2. Hauptsatz zur Hilfe nehmen, der uns sagt, dass die Entropie eines abgeschlossenen Systems im Gleichgewicht ihr Maximum annimmt. (Ja, ich weiß, ich habe immer noch nicht erklärt, was die Entropie eigentlich ist…) Nehmen wir an, das eine System hat eine bestimmte Energiemenge, das andere auch. Wenn ich die Gesamt-Entropie jetzt erhöhen kann, indem ich Energie vom einen System aufs andere übertrage, dann war ich vorher offensichtlich noch nicht im Gleichgewicht, denn die Gesamtentropie hat ja jetzt zugenommen. Wenn die Entropie maximal ist, dann muss gelten, dass sich die Gesamtentropie nicht mehr ändern lässt, indem ich Energie vom einen System auf das andere verschiebe – was das eine System an Entropie verliert, muss das andere an Entropie gewinnen.
Nehmen wir an, ich klaue dem einen System eine Energie ΔE zu und seine Entropie verringert sich um Δ S. Diese Energie füge ich jetzt dem anderen System zu. Dann muss entsprechend die Entropie des anderen Systems um ΔS zunehmen (und die Energie natürlich auch um ΔE), sonst würde sich die Entropie insgesamt ändern und wir wären nicht im thermodynamischen Gleichgewicht. Die Systeme tauschen also so lange Energie aus, bis sich die Entropie nicht mehr durch Austauschen von Energie erhöhen lässt.
Nach dem Nullten Hauptsatz muss das jetzt immer noch funktionieren, wenn wir eins unserer beiden Systeme mit einem dritten in Kontakt bringen, das dieselbe Temperatur hat (weil es dann auch mit dem im Gleichgewicht ist). Das bedeutet, dass für jedes System, das eine bestimmte Temperatur hat, gelten muss, dass seine Entropie um den Betrag ΔS zunimmt, wenn ich die Energie im den Betrag ΔE erhöhe. Die Größe ΔS/ΔE (die Entropie, die ich pro zugeführter Energiemenge bekomme) ist also für alle Systeme, die dieselbe Temperatur haben, gleich, sie muss also direkt von der Temperatur und von nichts anderem abhängen. Und so ist es auch; mit etwas mehr Mühe und Sorgfalt (ich empfehle das Thermodynamikbuch von Reif) kann man zeigen, dass die Beziehung so aussieht:
(In Physikbücher stehen da natürlich Differentiale statt der Deltas.)
Das ist also die Temperatur: Sie (beziehungsweise ihr Kehrwert) gibt an, um wie viel sich die Entropie eines Systems ändert, wenn ich ihm Energie zufüge. Ist die Änderung groß, dann ist die Temperatur niedrig, ist die Änderung klein, dann ist die Temperatur hoch. An der Gleichung sieht man auch, dass die Temperatur unendlich groß wird, wenn sich die Entropie bei Energiezufuhr gar nicht ändert, und sie wird schließlich negativ, wenn die Entropie kleiner wird, wenn ich dem System Energie zufüge.
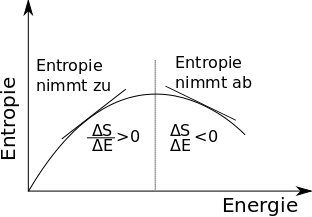
Um das etwas genauer zu sehen, nehmen wir an, die Entropie als Funktion der Energie verläuft so wie in dieser Kurve hier:
Die Änderung der Entropie mit der Energie ist nichts als die Steigung der Kurve. Anfänglich ist sie groß, die Temperatur ist also niedrig, weil sie ja der Kehrwert der Änderung ist. Später wird die Steigung immer flacher, die Temperatur wird also größer. Dann, genau an der gestrichelten Linie, hat die Entropie ein Maximum. Hier ist die Steigung gleich Null, die Temperatur ist unendlich groß, Und dann wird die Steigung negativ. Direkt hinter dem Maximum ist sie negativ, aber sehr flach, die Temperatur ist also negativ, hat aber einen hohen Betrag. Das System springt also von der Temperatur plus unendlich zu minus unendlich. Fügt man weitere Energie zu, wird die Steigung steiler, der Betrag der Temperatur sinkt also, sie nimmt von minus unendlich aus immer größere Werte (also solche mit kleinerem Betrag) an.
Man erreicht also negative Temperaturen, wenn man einem System, das eine Entropiekurve wie die gezeichnete hat, immer mehr Energie zufügt.
Tja, vom Standpunkt der theoretischen Thermodynamik aus gesehen ist das eigentlich schon alles, was es zur negativen Temperatur zu sagen gibt.
Schön wäre natürlich, man hätte eine Idee, was die Entropie genau ist und wie ein System aussehen muss, damit es eine Kurve wie die gezeichnete hat. Aber das verbanne ich in einen zweiten Teil…






Kommentare (31)