Hinweis: Dieser Artikel ist ein Beitrag zum ScienceBlogs Blog-Schreibwettbewerb 2015. Hinweise zum Ablauf des Bewerbs und wie ihr dabei Abstimmen könnt findet ihr hier. Informationen über die Autoren der Wettbewerbsbeiträge findet ihr jeweils am Ende der Artikel.

——————————————
1953 wurde die Struktur der DNA aufgeklärt und läutete eine Revolution in der Biologie ein. Etwa zur selben Zeit erlebten die Lebenswissenschaften eine weitere Umwälzung, die weniger bekannt ist: die erste menschliche, potentiell unsterbliche Zelllinie wurde etabliert. So gut wie alle Biologen, die ich kenne, haben im Laufe ihres Studiums oder ihres Berufslebens bereits mit diesen Zellen gearbeitet. Die Geschichte dahinter ist aber vielen – und war auch mir lange – unbekannt. Dabei ist sie wirklich faszinierend und wirft viele medizinisch-ethische Fragen auf wie z. B.: Was von meinem Körper gehört mir? Glücklicherweise schildert Rebecca Skloot in ihrem 2010 erschienenen Buch The immortal life of Henrietta Lacks (auf Deutsch: Die Unsterblichkeit der Henrietta Lacks), unter welchen Umständen die Zelllinie entwickelt wurde und welche Folgen das hatte.
1951 litt Henrietta Lacks, die aus ärmlichen Verhältnissen stammte, an starken Unterleibsblutungen und suchte das Johns Hopkins Hospital auf, weil es damals eines der wenigen Krankenhäuser war, das auch Schwarze behandelte. Wie sich herausstellte, hatte Henrietta Gebärmutterhalskrebs, der drei Monate zuvor, nach der Geburt ihres fünften Kindes, anscheinend noch nicht da war. Er musste also sehr schnell gewachsen sein. Während ihrer ersten Behandlung wurde eine Biopsie des Tumors gemacht und die Probe an George Gey weitergegeben.
Dieser versuchte damals bereits seit langem eine menschliche Zelllinie zu etablieren, das heißt: menschliche Zellen, die sich im Reagenzglas – außerhalb des Körpers – unendlich oft vermehren können. Während Zellen aller anderen Gewebeproben von Patienten bereits nach kurzer Zeit starben, vermehrten sich Henriettas Zellen unglaublich schnell und wuchsen bei konstanter Versorgung mit Nährstoffen einfach immer weiter. Gey nannte die Zelllinie HeLa, nach den Initialen von Henrietta Lacks.
Außerdem verteilte er die unsterblichen Krebszellen unentgeltlich an viele Kollegen und verschickte sie über die ganze Welt. Die Untersuchung menschlicher Zellen im Reagenzglas eröffnete fast unüberschaubar viele Möglichkeiten. Man testete an den Zellen die Auswirkungen von Toxinen, Arzneimitteln, Salmonellen oder radioaktiver Strahlung. In der Kosmetikindustrie dienten sie als Ersatz für Tierversuche. HeLa-Zellen waren auch an Bord des zweiten Satelliten überhaupt im Orbit, um zu untersuchen, wie sie auf Schwerelosigkeit und den Weltraumaufenthalt reagieren.
Und sie wurden massiv genutzt, um Viren zu untersuchen. HeLa-Zellen ließen sich mit verschiedenen Viren wie z. B. Polio infizieren. Das war genau das, was Jonas Salk brauchte, um seinen Polio-Impfstoff zu testen. HeLa ließ sich mit dem Virus und dem Blutserum potentiell immunisierter Menschen vermischen. War die Impfung wirksam, wurden die Zellen nicht infiziert, da die Antikörper des Serums die Viren inaktivierten. HeLa trug also auch maßgeblich zur Entwicklung des Polio-Impfstoffes bei. Um die riesigen Mengen des benötigten Zellmaterials herzustellen, wurde zum ersten Mal eine “Zellfabrik”, ein Gebäude allein zum Kultivieren von Zellen, gebaut und die Proben wurden gegen Geld verschickt.
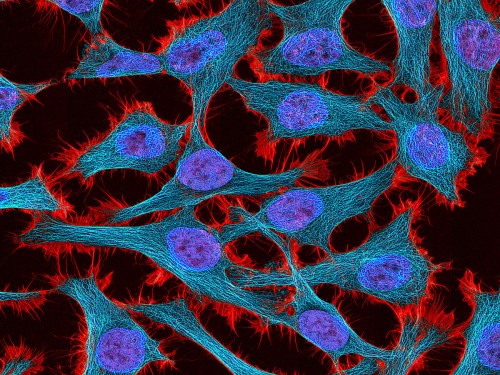
HeLa-Zellen unter dem Mikroskop. Zu sehen sind verschiedene Strukturproteine in Rot und Cyan sowie der Zellkern in blau. Bild: NIH, public domain.
Bei aller Euphorie um HeLa gab es aber auch Probleme, die im Buch ausführlich thematisiert werden. Eines war wissenschaftlich-technischer Art. Im Laufe der Zeit wurden immer mehr Zelllinien unterschiedlicher Herkunft etabliert, die sich aber nach und nach alle ähnlicher wurden. Wie sich irgendwann herausstellte, waren viele von ihnen kontaminiert – und zwar mit HeLa. Die Zellen wuchsen so gut, dass die anderen Zelllinien ihnen bei einer Kontamination nicht gewachsen waren. Viele Wissenschaftler erforschten also gar nicht die Zellen, für die sie sich eigentlich interessierten. Jahre an Forschung und Millionen von Dollar gingen so verloren.
Wie Rebecca Skloot in ihrem Buch auf eindringliche Art und Weise schildert, waren andere Probleme ethischer Natur. Die Injektion von HeLa-Zellen in Mäuse löste dort eine Tumorbildung aus. War das auch im Menschen möglich oder waren diese dazu fähig den Krebs zu bekämpfen? Der Onkologe Chester Southam spritzte in den 1950er Jahren teilweise unwissenden Patienten oder Gefängnisinsassen HeLa-Zellen. Je nach Zustand ihres Immunsystems entwickelten die Probanden Knoten unter ihrer Haut, die in Einzelfällen auch metastasierten, oder sie waren fähig die Zellen abzutöten. Das Ganze wurde erst gestoppt, als sich mehrere jüdische Ärzte weigerten, die Studien fortzuführen. Sie waren sich der Problematik bewusst, da sie die Nürnberger Prozesse verfolgt hatten und von den abscheulichen “Medizin”-Versuchen der Nazis wussten.
Zudem war auch Henrietta Lacks nie um Erlaubnis gefragt worden, ob ihr Gewebe für derartige Forschung verwendet werden darf. Etwas wie eine informierte Einverständniserklärung gab es damals noch nicht. Der Krebs kam nach ihrer Behandlung auch stärker zurück denn je und sie verstarb 1951 im Alter von 31 Jahren. Sie erfuhr nie von den Zellen, die nach ihr benannt sind. Und auch ihre Familie blieb zunächst unwissend. Erst 20 Jahre nach Henriettas Tod wurde ihr richtiger Name in Verbindung mit der Zelllinie veröffentlicht und zwei Jahre später erfuhr zufällig ihre Familie schließlich davon.
Den ärmlichen Verhältnissen und entsprechend geringer Bildung geschuldet, konnten die Familienmitglieder das Erzählte nicht richtig einordnen. Sie dachten, ein Teil von Henrietta – und nicht nur ihre Krebszellen – lebt wirklich, womöglich sogar in verschiedenen Kopien, da sie den Begriff Cloning in diesem Zusammenhang falsch verstanden. Und als sie hörten, dass man Gifte, HIV und radioaktive Strahlung an HeLa testet, vermuteten sie, dass ihre Verwandte tatsächlich noch leidet.
Rebecca Skloot lässt in ihrem Buch die Familienmitglieder ausführlich zu Wort kommen. Es wird klar, dass sich niemand darum bemüht hat, die Familie aufzuklären, die außerdem aufgebracht war, weil viele Menschen viel Geld mit HeLa verdient und ihre Karrieren vorangebracht haben, während Henriettas Hinterbliebenen leer ausgingen und sich die Gesundheitsversorgung kaum leisten konnten. Stattdessen wurden Blutproben von Henriettas Verwandten entnommen, um mehr über die Zelllinie herauszufinden. Diesen wurde aber nicht erklärt, was da vor sich geht, und sie vermuteten, dass sie auf Krebs getestet werden. Als sie einen der Wissenschaftler um Erklärungen zur Zelllinie baten, wurde ihnen ein vom Forscher verfasstes Genetik-Lehrbuch geschenkt. Natürlich signiert. Anfangen konnten sie damit allerdings nichts. Danach wurden genetische Daten der Verwandten in Science veröffentlicht, ohne Wissen oder Zustimmung der Betroffenen. Ähnliches passierte mit Teilen von Henriettas Patientenakte.

Eine Gedenktafel für Henrietta Lacks in der Nähe ihres Grabes. Bild: Emw, CC BY-SA 3.0.
Auch Henriettas Tochter Elsie hatte unter den damaligen Zuständen in Medizin und Wissenschaft zu leiden. Bei ihr war eine geistige Behinderung diagnostiziert worden und sie kam in das Hospital for the Negro Insane in Crownsville, in dem sie einige Jahre später verstarb. Skloot besuchte das Crownsville Hospital Center, wie es inzwischen hieß, mit Henriettas Tochter Deborah. Die beiden erfuhren, dass damals an womöglich fast allen Kindern dort für eine Epilepsiestudie eine sog. Pneumoencephalographie durchgeführt worden war. Um an scharfe Röntgenbilder des Schädelinneren zu kommen, war den Patienten die Hirnflüssigkeit entfernt worden, was mit starken Nebenwirkungen wie Übelkeit, Krampfanfällen und starken Kopfschmerzen einherging – das dauerte nach der Behandlung für mehrere Monate an, bis der Körper die fehlende Flüssigkeit wieder ersetzt hatte. Ziemlich sicher lagen auch hier nie Einverständniserklärungen vor.
Zwei von Henriettas Kindern erfuhren mit Skloots Hilfe schließlich doch noch genauer, was es mit den Zellen ihrer Mutter auf sich hat. Der damals an der Johns Hopkins University tätige Christoph Lengauer zeigte ihnen, wie die Zellen gelagert werden und wie sie unter dem Mikroskop aussehen. Außerdem erfuhren sie zum ersten Mal, dass HeLa ausschließlich aus Tumorzellen besteht und es keine “normalen” Zellen ihrer Mutter sind. Und zumindest Henriettas Tochter Deborah, die noch vor Veröffentlichung des Buches verstarb, scheint mit der Geschichte ihren Frieden gemacht zu haben.
Und was ist nun die Antwort auf die eingangs gestellte Frage, was von meinem Körper mir gehört? Habe ich das Recht darüber zu verfügen, was mit Zellen oder Gewebe passiert, das meinem Körper entnommen wurde? Oder ist es Eigentum des Arztes oder der Klinik? Skloot erwähnt, dass in Amerika ein Gericht im Jahr 1990 festgestellt hat, dass Biopsiematerial nicht mehr Eigentum des Patienten ist. Ob das Urteil noch aktuell ist, weiß ich allerdings nicht. Zur Situation in Deutschland schreibt das Deutsche Krebsforschungszentrum: “Frisches, eingefrorenes oder in Paraffin konserviertes, aber ansonsten nicht weiter bearbeitetes Gewebe bleibt das Eigentum des Patienten”, dass dies aber nicht mehr so klar sei, “wenn ein Patient der Entnahme und Weiterverarbeitung von Gewebe zu wissenschaftlichen Zwecken zugestimmt hat”. Vielleicht weiß einer der Mitlesenden mehr? Henrietta Lacks und viele andere Menschen jedenfalls wurden sowieso nie gefragt.
In den USA gibt es inzwischen die Henrietta Lacks Foundation und vielleicht wird die Geschichte sogar verfilmt. Mein Eindruck ist aber leider, dass diese Episode der Medizingeschichte in Deutschland weniger bekannt ist. Dabei zeigt The immortal life of Henrietta Lacks, das auch auf Deutsch erhältlich ist, auf eindrückliche und einfühlsame Weise, zu welchen Fortschritten Medizin und Wissenschaft fähig sind – aber auch dass viele Menschen für diese Fortschritte einen hohen Preis bezahlt haben. Man erhält einen Einblick, was alles passieren musste, damit das Konzept der informierten Einwilligung verpflichtend wurde. Rebecca Skloot hat mit ihrem Buch einer Frau und ihrer Geschichte ein Denkmal gesetzt, das so viele Leser wie möglich verdient hat.
————————————————-
Hinweis zum Autor: Dieser Artikel wurde von “Böx” veröffentlicht: “Böx ist Biologe und teilt seine Leseeindrücke seit einiger Zeit auf seinem Bücherblog”












Kommentare (18)