Ich habe noch nicht sehr viel über Epigenetik geschrieben, dabei ist das Thema höchst interessant. Epigenetik ist inzwischen längst auch für die forensische Genetik von Bedeutung und mein Team und ich werkeln gerade an einem ersten Forschungsansatz. Es ist also höchste Zeit, in einem Basics-Artikel ein wenig von den Grundlagen der Epigenetik zu erklären. (Zur Vorbereitung der Lektüre dieses Artikels empfiehlt sich bei Bedarf die Auffrischung der Kenntnisse über DNA). Das Wort „Epigenetik“ mit seiner griechischen Vorsilbe „Epi“ (für „um …herum“ oder „zusätzlich zu“) bezeichnet Vorgänge, Phänomene und Prozesse, die als zusätzlich zur „klassischen“ Genetik aufgefasst werden können, wenn man unter letzterer einmal die Kodierung von Aminosäuren in der Abfolge (=Sequenz) der Nukleotide der DNA und die Vererbung nach den Mendelschen Regeln versteht.
Epigenetische Veränderungen betreffen daher nicht die Nukleotidsequenz, also den eigentlichen Inhalt des Genoms, sondern z.B. die Entscheidung, ob und/oder in welcher Reihenfolge bestimmte Passagen des Genoms abgelesen, ob und wann also ein Gen exprimiert wird oder nicht. Sie können so erheblichen Einfluss auf die Funktion eines Gens und das Erscheinungsbild (Phänotyp) einer Zelle ausüben und sie sie können auch auf Tochterzellen und möglicherweise sogar Abkömmlinge eines Organismus vererbt werden.
Ich habe schon einen Basics-Artikel zur Regulation der Genexpression geschrieben, durch Nachlesen dessen man die Notwendigkeit und Bedeutung der differentiellen Genaktivität noch einmal rekapitulieren kann. Noch einmal ganz kurz: da (bis auf wenige Ausnahmen) jede Zelle das gesamte Erbgut eines mehrzelligen Organismus enthält, von dieser riesigen Informationsmenge jedoch nur einen Bruchteil für die Ausübung ihrer eigentlichen Funktion benötigt, muß eine menschliche Zelle (durch innere und äußere Einflüsse) genau steuern, welche der über 20.000 Gene zu welchem Zeitpunkt ausgeprägt (= exprimiert) werden, um sie mit genau den Genprodukten zu versorgen, die sie in jedem Moment gerade benötigt. Die zur Verfügung stehenden Steuerungsmechanismen der Genexpression sind vielfältig und kompliziert und epigenetische Veränderungen gehören dazu.
Wenn wir noch einmal die Restaurantanalogie aus jenem Basics-Artikel hernehmen und uns die DNA wie ein Kochbuch vorstellen mögen, dann entsprächen genetische Veränderungen (= Mutationen) also Änderungen im Text der Rezepte, wohingegen epigenetische Veränderungen eher an den Rand gekritzelten Anmerkungen und Büroklammern entsprächen, die hier und da Seiten zusammenhalten, so daß sie nicht aufgeschlagen und abgelesen werden können. Man kann sich leicht vorstellen, daß beide Arten von Veränderungen einen große Auswirkung auf das spätere Ergebnis haben können, ob nun in einem Rezept „Zucker“ durch „Salz“ ersetzt wird (Mutation) oder ein Gala-Dinner nur aus Suppe und Nachtisch ohne Hauptgang besteht (epigenetische Veränderung).
Nun gibt es ganz verschiedene Mechanismen zur epigenetischen Regulation und man kann sogar die Interferenz bei der Genexpression durch kleine RNAs (RNAi), zu denen auch mein Liebling, die miRNA, gehört, dazu zählen. Neben RNAi sind besonders wichtige Mechanismen aber die Methylierung von DNA-Nukleotiden und die Modifikation von Histon-Proteinen.
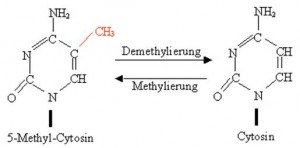 Methylierung bedeutet das chemische Anfügen einer Methylgruppe, -CH3 (s. Abbildung ). Epigenetische Veränderungen in Form von DNA-Methylierungen betreffen dabei immer nur Cytosin-Nukleotide und besonders dann, wenn diese in Sequenzumgebungen vorkommen, die reich an der Nukleotidabfolge Cytosin-Guanin (CG) sind, die sogenannten „CpG-Inseln“. Die Anfügung der Methylgruppe übernimmt dabei das Enzym DNA-Methyltransferase (DNMT). Aber wie kommt man nun von methylierten Cytosinen zur Steuerung der Genregulation?
Methylierung bedeutet das chemische Anfügen einer Methylgruppe, -CH3 (s. Abbildung ). Epigenetische Veränderungen in Form von DNA-Methylierungen betreffen dabei immer nur Cytosin-Nukleotide und besonders dann, wenn diese in Sequenzumgebungen vorkommen, die reich an der Nukleotidabfolge Cytosin-Guanin (CG) sind, die sogenannten „CpG-Inseln“. Die Anfügung der Methylgruppe übernimmt dabei das Enzym DNA-Methyltransferase (DNMT). Aber wie kommt man nun von methylierten Cytosinen zur Steuerung der Genregulation?
Man kann sich so eine Methylierung wie eine Markierung oder (etwas bildlicher) wie diese Kunststoffstacheln, die manche Gebäude zur Abwehr von Tauben auf den Dachfirsten angebracht haben, vorstellen. Zur Genregulation werden nämlich Cytosine methyliert, die in einer Promotorregion eines Gens liegen. Der Promotor ist so etwas wie der Startblock für die Transkription, an dem sich die RNA-Polymerase und alle sonst noch nötigen Proteine (z.B. Transkriptionsfaktoren) treffen und für die Transkription bereit machen. Wenn man sich die RNA-Polymerase nun wie eine Taube vorstellt, die sich gemütlich auf der DNA niederlassen möchte, dann wird sie von den „Methylgruppenstacheln“ auf den Cytosinen daran gehindert: sie kann sich nicht setzen und fliegt wieder weg; es gibt keine Transkription und das Gen wird nicht aktiviert. Methylierte Cytosine in Promotorregionen sind also (fast immer) Markierungen für inaktivierte Gene.



Kommentare (85)