Heute werde ich mich mit einer (nicht mehr ganz so) neuen aber immer noch revolutionären molekularbiologischen Technik zur Editierung also Veränderung und Anpassung von Genen befassen. Im Jargon wird sie kurz als CRISPR (ausgesprochen „krisper“) bezeichnet, was im Englischen zugleich ein Wortspiel ist, wo „crisper“ so viel wie „knackiger“ bedeutet und wie schon über NGS sagen manche Forscher über CRISPR bereits jetzt, daß seine Bedeutung für molekulare Biologie und Genetik derjenigen der PCR gleichkommen wird, z.B. Rudolf Jaenisch, der sie als „game changer“ sieht. In der Tat: CRISPR ist dabei, die Gentechnik zu revolutionieren und vor allem zu demokratisieren, da die Geneditierung mit CRISPR so leicht, schnell und preisgünstig ist, daß nun auch kleine und „unerfahrene“ Labore damit arbeiten können.
Einige Sciencebloggerkollegen haben sich auch schon mit CRISPR befasst, mein eigenes Interesse für CRISPR rührt allerdings nicht nur daher, daß es derzeit so einen Hype darum gibt und es in der Tat eine unglaublich spannende, coole und flexible Technik ist, sondern ist insofern auch biographisch geprägt, als ich in meiner Diplomarbeit selber und mühselig die Genome von Adenoviren editiert und ein Gen des Malariaerregers P. falciparum darin eingebaut habe, um mit diesen nicht mehr pathogenen, „transgenen“ Viren dann Mäuse zu infizieren, woraufhin diese eine Immunantwort gegen Malaria ausprägten (ich wollte dadurch mithelfen, einen Malaria-Impfstoff herzustellen). Hätte ich damals schon CRISPR gehabt, hätte ich ein paar Nachtschichten weniger schieben müssen 🙂
Was ist CRISPR?
CRISPR ist eigentlich ein Akronym das für „Clustered Regularly Interspaced Short Palindromic Repeats“ steht und kurze, palindromische DNA-Sequenzwiederholungen bezeichnet, die sich im Genom vieler Bakterien und Archaeen befinden und durch kurze Abstandshalter (“spacer”) voneinander getrennt sind.
Entdeckt hat man diese Sequenzen schon im Dezember 1987 in E. Coli-Bakterien aber genau wie bei der mirco-RNA, die man 1993 im Fadenwurm C.elegans entdeckte, verstand man damals nicht, was man da vor sich hatte, hielt es für unbedeutend und kümmerte sich nicht weiter darum. Erst als im Juli 1995 klar wurde, daß es CRISPR-Sequenzen auch in vielen anderen Mikroorganismen gibt, wurde man aufmerksam. Und doch dauerte es bis 2007, bis man erkannte, daß diese Sequenzen offenbar Teil einer Art bakteriellen Immunsystems sind.
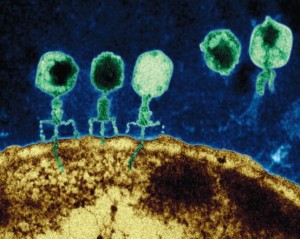
Ja, ganz recht, ein bakterielles Immunsystem! In der Lebensmittelindustrie werden für bestimmte Verarbeitungsprozesse von Milchzucker Streptococcus thermophilus (S. thermophilus) Bakterien verwendet. Diese können jedoch von bakterienfressenden Viren, sogenannten Bakteriophagen, befallen und getötet werden und eine solche sich rasch ausbreitende Infektion kann ganze Produktionschargen verderben.
In einer dänischen Firma für Nahrungsmittelzusätze fand man heraus, daß man S. thermophilus gegen Bakteriophagen immunisieren, sozusagen impfen kann, indem man die Bakterien vor der Prodution dem Phagen aussetzte. Diese Behandlung schützte die Bakterien danach wirkungsvoll vor den Viren [1].
Aber wie machen die Bakterien das? Wie können prokaryotische Einzeller eine adaptive Immunantwort zustandebringen, wofür unsereins einen hochkomplexen und zahlreiche Zelltypen umfassenden Mechanismus benötigt? Ganz grob gesagt: das Bakterium speichert einen kurzen Ausschnitt aus der Phagen-DNA in seinem eigenen Genom, nämlich als die oben erwähnten “Spacer” zwischen den palidromischen Sequenzen (also dem CRISPR-Bereich) und wenn das Bakterium später erneut von einem solchen Phagen infiziert wird, wird dessen DNA anhand der im CRISPR-Bereich gespeicherten Sequenzen und mithilfe eines speziellen Enzyms, genannt Cas, gezielt zerlegt und der Phage somit unschädlich gemacht.
____
Referenz:
[1 ] Barrangou, R., Fremaux, C., Deveau, H., Richards, M., Boyaval, P., Moineau, S., … & Horvath, P. (2007). CRISPR provides acquired resistance against viruses in prokaryotes. Science, 315(5819), 1709-1712.
__
Nachtrag am 07.10.2020: Völlig verdient erhalten dieses Jahr Emmanuelle Charpentier und Jennifer Doudna den Nobelpreis in Chemie für ihre Entdeckung!



Kommentare (15)